Disponer de alimentos mejorados, vegetales y animales resistentes a plagas o enfermedades, obtener nuevas generaciones de medicamentos más eficaces y económicos, comprender más profundamente enfermedades que hasta hoy son arcanos, generar en el futuro órganos para trasplantes y hasta lograr, rápidamente, un antídoto contra una epidemia global de aparición sorpresiva. Algunos de estos objetivos constituyen hoy logros efectivos, y muchos de los otros ya no son producto de afiebrados guionistas de películas futuristas de ciencia ficción. Detrás de todo ello está la biotecnología moderna.
La biotecnología se conoce hace muchísimos años y puede definirse como la parte de la ciencia que estudia y desarrolla el uso de organismos vivos con diferentes fines. No obstante, el término “biotecnología moderna” nace más específicamente a mediados de la década de 1970, cuando se descubren, aíslan y caracterizan los diferentes tipos de enzimas de restricción, las que pueden “cortar” el ADN en secuencias específicas.
En virtud de este y otros hallazgos, que con posterioridad contribuyeron a consolidar el entendimiento de lo que hoy conocemos como tecnología del ADN recombinante (o clonación de genes) e ingeniería genética, las moléculas de ADN de dos o más fuentes diferentes se pueden combinar para generar organismos genéticamente modificados.
La obtención de alimentos con características nutricionales mejoradas, el desarrollo de especies vegetales y animales resistentes a ciertas plagas o enfermedades, la comprensión de los factores moleculares involucrados en enfermedades de base genética, la posibilidad de acceder a órganos para trasplante, la transformación y eliminación de agentes contaminantes para el medioambiente, la producción de una nueva generación de medicamentos e inclusive la obtención de un antídoto eficiente ante la emergencia de una futura epidemia son solamente algunos ejemplos de las aplicaciones puntuales que la biotecnología podría tener.
EL PHARMING: LA METÁFORA DE LOS REBAÑOS ANIMALES Y LOS CULTIVOS VEGETALES DE GRANJA COMO VERDADERAS FARMACIAS VIVIENTES
Etimológicamente, el término Pharming es un neologismo que deriva de un juego de dos palabras en inglés: farming (que alude al cultivo en granjas) y pharmacy (que significa farmacia). Bajo esta denominación se designa a un grupo creciente de técnicas empleadas para obtener productos bioterapéuticos (más precisamente proteínas recombinantes, tales como anticuerpos monoclonales, antígenos vacunales, factores sanguíneos de la coagulación, hormonas, factores de crecimiento y citoquinas, por nombrar solamente algunos) a partir de grandes animales o de plantas, típicamente de granja.
En este contexto, y gracias al avance en la comprensión y el desarrollo de las más sofisticadas herramientas biotecnológicas combinadas con el conocimiento de la fisiología animal y vegetal, un pequeño rebaño porcino, bovino, caprino, o unas pocas hectáreas de cultivo podrían satisfacer potencialmente las necesidades terapéuticas de millones de pacientes de todo el mundo.
Existe un gran número de hechos a favor de la obtención de medicamentos biotecnológicos a partir de la utilización de grandes animales o plantas transgénicos. En general, uno de los factores que más contribuye al crecimiento del mercado biofarmacéutico es el aumento de la demanda de proteínas recombinantes. En relación a esto, la provisión de insulina para los pacientes diabéticos es un ejemplo. Se ha estimado que en el año 2000, alrededor de 171 millones de personas padecían diabetes mellitus tipo 1 o 2 en todo el mundo, y se considera que esta cifra aumentará a 366 millones en 2030. Aunque solamente una fracción de los diabéticos requiere insulina, la necesidad de esta proteína aumentará indudablemente.
En segundo lugar, los medicamentos bioterapéuticos formulados con anticuerpos monoclonales representan uno de los campos más promisorios y, en consecuencia, su desarrollo ha venido creciendo exponencialmente en los últimos años. En forma comparativa, se ha estimado que los costos de producción (por gramo de anticuerpo monoclonal, con una tasa de producción anual de 100 kg/año) son más bajos en maíz transgénico y cabras transgénicas que en los sistemas de producción tradicionales. Por último, los grandes animales transgénicos (principalmente, pero también en menor medida las plantas transgénicas) proporcionan un medio adecuado para producir proteínas que son difíciles de generar de otras maneras.
Muchas de las proteínas terapéuticas para uso en humanos requieren de modificaciones complejas, posteriores a su “fabricación” en el interior celular para que puedan actuar en forma apropiada, las cuales difícilmente se puedan lograr en la mayoría de los microorganismos o en células de mamíferos cultivadas. A este respecto, una de las modificaciones más críticas queda representada por la adición de azúcares a las proteínas, proceso denominado glicosilación: los patrones de glicosilación son bastante diferentes entre bacterias, levaduras, plantas y mamíferos, y esto puede tener profundas consecuencias farmacológicas e inmunológicas para los pacientes.
LOS ANIMALES DE GRANJA COMO PLATAFORMA PARA OBTENER MEDICAMENTOS
La lista de animales transgénicos utilizados para obtener proteínas recombinantes ha venido creciendo en los últimos años. Respecto de las especies mamíferas, el cerdo, el conejo, la oveja, la cabra y la vaca posiblemente sean los ejemplos más representativos. Respecto de las aves, el pollo doméstico (Gallus gallus domesticus) es la especie que más ha sido investigada.
La glándula mamaria como biorreactor
De todos los potenciales fluidos biológicos mamíferos en los que se puede expresar la proteína de interés, la leche constituye el más estudiado y el único que ha podido ser desarrollado a gran escala hasta la actualidad. Esto es así porque la glándula mamaria totalmente desarrollada tiene una enorme capacidad para fabricar proteínas. Además, la industria lechera está bien establecida no solo para el ganado bovino sino también para las ovejas y cabras. Por lo tanto, los conocimientos necesarios para la recolección, el procesamiento y la purificación de la leche en animales transgénicos ya cuentan con un antecedente industrial y son favorablemente aprovechados.
La importancia de la glándula mamaria como biorreactor cobra máxima trascendencia al revisar la historia de los dos primeros medicamentos formulados con una proteína recombinante transgénica: a) ATryn®, de GTC Biotherapeutics (actualmente rEVOBiologics), que incluye antitrombina recombinante humana (rhAT) como principio activo, obtenida a partir de la leche de cabra, empezó a comercializarse en el año 2006 en el mercado europeo y tres años más tarde en el estadounidense; y b) Ruconest®, de la empresa holandesa Pharming, que contiene conestat alfa (un inhibidor de la esterasa C1 humano recombinante o rhC1INH), obtenido a partir de leche de conejo, se aprobó en octubre del año 2010 en el mercado europeo y cuatro años más tarde en el estadounidense.

Fotografía de ATryn®, el primer medicamento transgénico aprobado para uso en humanos
Actualmente se obtiene en la Argentina un alto nivel de expresión de la hormona de crecimiento recombinante humana (recombinant human growth hormone o rhGH) (hasta 5 gramos por litro) en la leche de vacas transgénicas.
El huevo aviar como biorreactor
Los huevos de pollo tienen varias ventajas que los hacen atractivos para la producción de proteínas foráneas: a) la industria avícola está ampliamente desarrollada y las razas modernas de pollos son altamente productivas; b) la recolección de huevos es muy simple; c) se pueden obtener grandes cantidades de animales transgénicos a partir de un solo macho transgénico; d) el uso de huevos con fines farmacéuticos ya está establecido para la producción de vacunas, proporcionando un marco regulatorio para las proteínas recombinantes transgénicas; y e) el perfil de glicosilación de las proteínas humanas y aviares son altamente similares.
El 8 de diciembre de 2015 la Food and Drug Administration (FDA) aprobó Kanuma®, de la empresa Alexion Pharmaceuticals, que contiene como principio activo a la enzima sebelipasa alfa, obtenida y purificada a partir de la clara de huevo de gallinas transgénicas. El medicamento está indicado como terapia de reemplazo enzimático en pacientes de cualquier edad diagnosticados con alguna forma de deficiencia de la lipasa ácida lisosomal o LAL, una enfermedad metabólica extremadamente rara y de base genética.
LOS CULTIVOS VEGETALES COMO PLATAFORMA PARA OBTENER MEDICAMENTOS
El uso de plantas, o sus extractos, para el tratamiento de enfermedades humanas se remonta a miles de años A.C. En el siglo XVI, por ejemplo, los jardines botánicos funcionaban como verdaderas farmacias que proporcionaban una gran cantidad de sustancias con actividad terapéutica. Sin embargo, es gracias al desarrollo de la ingeniería genética y de la biotecnología moderna que las fuentes botánicas transgénicas han resurgido no solo para la producción de nuevos agentes medicinales sino también para la obtención de numerosas sustancias de aplicación en otras industrias diferentes de la farmacéutica.
La creación de las primeras plantas transgénicas se informó en 1983. Desde entonces, muchas proteínas recombinantes (tales como anticuerpos monoclonales, sustitutos de la sangre, hormonas, vacunas, factores de crecimiento, etc.) se han expresado en varias especies de importancia agronómica. De hecho, en los últimos años se ha acuñado el término plantibodies para designar a aquellos anticuerpos (en inglés antibodies) recombinantes derivados de plantas transgénicas.
Históricamente, la especie de elección para la producción de la mayoría de las proteínas recombinantes vegetales ha sido el tabaco (Nicotiana tabacum), una planta con hoja fácil de operar genéticamente. Sin embargo, hoy en día se utiliza un gran número de otras especies tales como la alfalfa, el tomate, la banana, el arroz, el maíz, el trigo, la zanahoria, la soja, la papa y la lechuga.
Entre los muchos órganos vegetales donde es más frecuente la expresión de proteínas transgénicas, las hojas, las semillas, las frutas y las raíces constituyen los ejemplos más habituales.
Plantas transgénicas versus animales transgénicos
En comparación con los animales, son muchas las razones que sustentan la utilización de las plantas transgénicas como plataforma para la obtención de medicamentos. A continuación se mencionarán algunas de las más destacadas.
- La generación de plantas transgénicas es relativamente más fácil, más eficiente y menos costosa que la de animales transgénicos.
- El desarrollo de la plataforma vegetal con fines médicos entraña la esperanza de minimizar el riesgo de transmisión de enfermedades mediadas por microorganismos o priones dañinos para el ser humano.
- Las plantas representan un adecuado biorreactor para sustancias muy activas en animales transgénicos, tales como la eritropoyetina y algunas citoquinas.
- Las plantas pueden proporcionar un vehículo ideal para la administración oral de antígenos vacunales debido a la presencia de pared celular gruesa, compuesta de celulosa y otros azúcares, capaz de suministrar protección contra la degradación por el tracto gastrointestinal.
- En líneas generales, las plantas transgénicas son socialmente mejor aceptadas que los animales transgénicos. A este respecto y a diferencia de la biotecnología “roja”, en la biotecnología “verde” no existe sufrimiento animal.
- La expresión de proteínas recombinantes en las semillas de las plantas ofrece la valiosa posibilidad de almacenarlas por largos periodos, sin necesidad de recurrir a procesos o equipos costosos.
A pesar de las bondades de las plantas transgénicas mencionadas arriba, la desventaja más sobresaliente queda constituida por el perfil de glicosilación de las proteínas vegetales recombinantes. En otras palabras, las plantas utilizan unidades de azúcares diferentes de las que usan las células de mamíferos en la fabricación de sus glicoproteínas, lo que podría llegar a ocasionar serios problemas de salud en los pacientes.
El advenimiento de los medicamentos obtenidos a partir de plantas transgénicas
La enfermedad de Gaucher resulta de la deficiencia parcial o total de una enzima lisosomal llamada glucocerebrosidasa, que cataliza la hidrólisis de un lípido complejo denominado glucocerebrósido. Es uno de los trastornos de almacenamiento lisosómico más comunes, afectando hasta 1 de cada 40.000 nacidos vivos en la población general. En mayo de 2012 comienza a comercializarse en Estados Unidos taliglucerasa alfa (Elelyso®, de Pfizer y Protalix BioTherapeutics), el primer medicamento aprobado por la FDA que incluyó un principio activo obtenido a partir de células vegetales transgénicas.
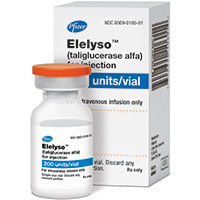
Fotografía de Elelyso®, el primer medicamento obtenido a partir de una plataforma vegetal transgénica y aprobado para uso en humanos
LAS DESVENTAJAS DEL PHARMING
El Pharming entraña una aproximación con un enorme potencial y, en teoría, ofrece importantes ventajas técnicas y económicas sobre los métodos de producción ya existentes: como se mencionó anteriormente, la posibilidad de obtener grandes cantidades de un principio farmacéuticamente activo de origen biotecnológico a un precio competitivo es una de las más seductoras.
Sin embargo, el Pharming también plantea una serie de cuestiones complejas e interrogantes sociales que aún no han sido completamente esclarecidos, relacionados principalmente con las objeciones alrededor de la manipulación del genoma de animales y plantas, la falta de conocimiento de la población general acerca de las técnicas biotecnológicas de transgénesis, las percepciones en torno al sufrimiento animal, las creencias religiosas y/o morales, la ausencia de generación de información de calidad desde las instituciones hacia la sociedad entera, la falta de un marco regulatorio específico y actualizado, la necesidad de conformar comités especiales y competentes, los niveles de confianza a las instituciones y las dificultades de evaluar y dimensionar potenciales riesgos a mediano y largo plazo.
Diego Canseco
Farmacéutico y primer Especialista en Biotecnología Bioquímico-Farmacéutica por la Universidad de Buenos Aires.
La nota está basada en el trabajo de investigación final “Productos biofarmacéuticos transgénicos: pasado, presente y futuro de las especialidades medicinales basadas en el Pharming”, que fue dirigido por la doctora Ana Sotelo.
Glosario
Anticuerpo monoclonal: proteína artificial producida en el laboratorio para unirse a un único tipo de sustancia. Solos o como vehículo para transportar medicamentos, toxinas o materiales radiactivos, los anticuerpos monoclonales se usan muy frecuentemente en la actualidad para tratar algunos tipos de cáncer.
Biorreactor: en el contexto del Pharming, un biorreactor es un tejido o un órgano de una especie transgénica determinada en donde se expresa y/o secreta la proteína de interés terapéutico.
Glicoproteínas: grupo particular de proteínas complejas que presentan en su estructura hidratos de carbono o azúcares. En los organismos que las expresan, cumplen funciones definidas, tales como el reconocimiento celular y la instrumentación de respuestas inmunes.
Organismo transgénico: organismo manipulado genéticamente que exhibe en su genoma uno o más genes que no forman parte de su repertorio genético original. Estos últimos son denominados transgenes, genes exógenos o foráneos.
Proteína recombinante: proteína obtenida a partir de cualquier técnica basada en la tecnología del ADN recombinante o clonación de genes.












Dejar un comentario